Page 28 - Libro de Ponencias Congres SEHH-SETH 2017
P. 28
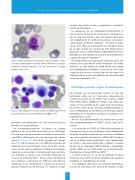
Figura 2. Falta de lobulación y fenómeno de la cromatina conden- sada en paciente diagnosticado de anemia refractaria con exceso de blastos y deleción del brazo corto del cromosoma 17. Sangre periférica. HE × 100.
Figura 3. Micromegacariocito en paciente con SMD e inversión del brazo largo del cromosoma 3. Médula ósea MGG × 100.
pacientes con alteraciones en 17p, han hecho que el término no se generalizara.
Los micromegacariocitos circulantes en sangre periférica son un evento muy raro que, sin embargo, ha sido descrito de manera recurrente en pacientes con SMD y alteraciones en el brazo largo del cromo- soma 3 (Figura 3)(9). Esta lesión aparece en menos de un 1% de los pacientes con SMD. Recientemente, Gröschel et al. encontraron como en el 98% de los casos en los que la neoplasia mieloide se acompa- ñaba de una inversión o translocación del cromoso- ma 3 existía, al menos, una mutación adquirida en un gen de la familia RAS(10). Existe cierta controversia en cuanto a si considerar los SMD con este tipo de alteración en el cromosoma 3 como una leucemia aguda mieloide ya de entrada, sin importar el por-
centaje de blastos, dado su pronóstico invariable- mente desfavorable.
La presencia de un cromosoma isodicéntrico X, con el punto de rotura en la banda 13 del brazo lar- go, ha sido descrita en casos de anemia refractaria con sideroblastos en anillo, en ocasiones asociada a cierto grado de brosis medular(11). En 2013 se publi- có en Cell cómo la inactivación en modelo murino de un gen situado en esa banda, XIST, provocaba la aparición de una enfermedad mieloproliferativa/mie- lodisplásica que reproducía con bastante delidad el cuadro descrito en humanos(12).
El síndrome de la condensación anómala de la cro- matina se ha descrito en varias entidades, en mielo- displasia, en LMC atípica o como efecto secundario al micofenolato de mofetilo. Y, aunque no se ha aso- ciado hasta la fecha a ningún gen en concreto, sí ha sido descrito en casos con deleción aislada del brazo corto del cromosoma 12(13).
❯ Mutaciones puntuales y signos de mielodisplasia
Los estudios de secuenciación masiva ya han de- terminado cuáles son las mutaciones adquiridas de manera recurrente en los SMD. Y hay 6 genes, SF3B1, TET2, SRSF2, ASXL1, DNMT3A y RUNX1, que están pre- sentes en más del 10% de los casos. Estas mutaciones frecuentes, junto con la conocida heterogeneidad clí- nica y morfológica de los SMD, ya nos anticipa que los fenotipos y las mutaciones somáticas se solapan en la mayoría de los casos.
Aun así, ha habido intentos de establecer una rela- ción genotipo-fenotipo en SMD(14), de los que desta- camos:
1. La mutación en SF3B1, en SMD, está asociada de manera casi exclusiva a la presencia de sideroblastos en anillo. La combinación de una mutación iniciadora con una mutación subclonal en JAK2 o MPL se asocia con la entidad anemia refractaria con sideroblastos en anillo y marcada trombocitosis (ARSA-T), incluida dentro de la categoría SMD/síndromes mieloprolife- rativos (SMP) en la clasi cación de la Organización Mundial de la Salud (OMS) de 2016(15).
2. Hasta la fecha, no se ha encontrado ninguna mutación característica de la categoría con displasia multilínea sin sideroblastos en anillo.
3. La citopenia refractaria con displasia multilínea y la anemia refractaria con exceso de blastos se aso-
LIX Congreso Nacional de la Sociedad Española de Hematología y Hemoterapia / Ponencias
28